3.1. 染色体与DNA¶
DNA控制生物性状遗传(少数以RNA为遗传物质,部分病毒、类病毒);RNA、DNA均以核苷酸 图 3.1.1 为基本单位,详阅5.1核酸结构。
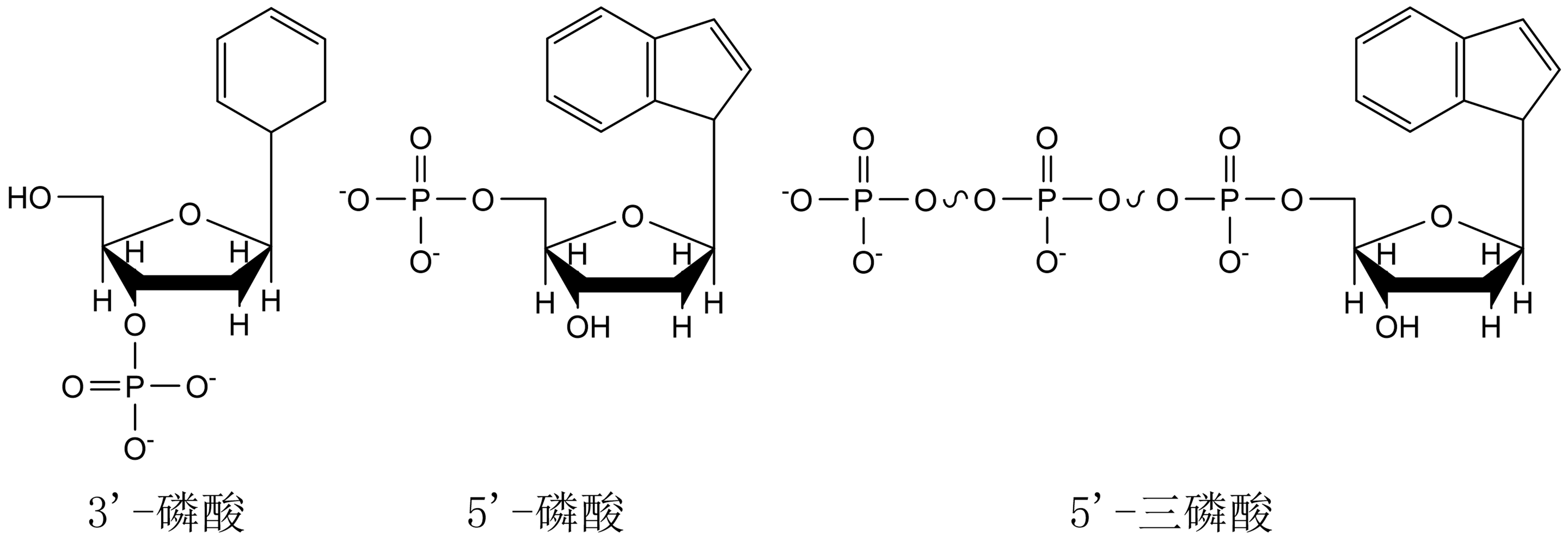
图 3.1.1 核苷酸组成结构¶
3.1.1. 染色体¶
染色体:包含DNA、蛋白质,亲代以染色体形式将遗传物质DNA传递至子代,保持物种稳定性、延续性。
同一物种每条染色体所带DNA量一定,但不同染色体或不同物种间差异明显。
组成染色体的蛋白质(组蛋白、非组蛋白)种类、含量稳定。
胞内DNA主要存于染色体上,而称染色体为遗传物质的主要载体。
特征 |
原核细胞 |
真核细胞 |
|---|---|---|
体积 |
小(1~10μm) |
较大(5~100μm) |
基因组 |
DNA与非组蛋白结合,于类核中 |
DNA与组蛋白、非组蛋白结合成染色体 |
分裂形式 |
裂殖、出牙 |
有丝、减数 |
被摸胞器 |
无 |
线粒体,叶绿体等 |
能量代谢 |
质膜氧化酶系 |
线粒体 |
细胞骨架 |
无 |
微管,中间纤维等 |
胞间运动 |
无 |
原生质流动胞饮 |
真核细胞中,染色体位于核仁内,呈极细微线性构造;在细胞周期中占较长时间的间期,以细且松散染色质于细胞核;DNA与蛋白质完全融合。
原核细胞无细胞核,DNA于类核结构拟核,外裹稀疏蛋白质(参与DNA折叠,复制、重组、转录)。
DNA主要特征:
常仅1条染色体且多带单拷贝基因,少数多拷贝(rRNA基因);
全染色体DNA几乎全为功能基因及调控序列;
几乎每个基因序列皆与所编码蛋白质序列线性对应。
3.1.1.1. 真核细胞染色体¶
真核细胞具明显核结构,染色体均为二倍体(生殖细胞外)。
生殖细胞(配子)染色体为体细胞一半,即单倍体;受精卵(合子)由精、卵细胞结合成。
染色体特征:
分子结构相对稳定;可自我复制,亲子代间保持连续性;
可指导蛋白质合成,控制整个生命过程;
可产生可遗传变异。
蛋白质构成:
组蛋白(进化极端保守性,无组织特异性,肽链氨基酸分布不对称,具多种修饰:甲基化、乙酰化、磷酸化、泛素化、ADP核糖基化等,组蛋白H5或与染色质失活相关);
非组蛋白(HMG蛋白、DNA结合蛋白、A24非组蛋白)。
基因组DNA:
不重复序列(常仅一个或几个拷贝,750~2kbp;结构基因基本属不重复序列);
中度重复序列(重复101~104,各种rRNA、tRNA、某些结构基因如组蛋白属此类);
高度重复序列(卫星DNA,仅于真核生物,6~100bp、串联重复成千上万次,多位于着丝粒处、部分于染色体臂,高度浓缩为异染色质组成,不转录)。
核小体:
由H2A、H2B、H3、H4各两分子成八聚体及约200bpDNA盘绕构成,H1于核小体外;
核心颗粒146bp、绕1.75圈(每圈约80bp)。
名称 |
构成 |
长度压缩(倍) |
|---|---|---|
核小体 |
DNA、组蛋白 |
7 |
螺线管 |
核小体 |
6 |
超螺旋 |
螺线管 |
40 |
染色体 |
超螺旋 |
5 |
合计 |
8k~10k |
基因组特点:
庞大,常远大于原核生物基因组;
存在大量重复序列;
大部分为非编码序列(与细菌、病毒间最主要区别);
转录产物为单顺反子;
基因为断裂基因,具内含子结构;
存在大量顺式作用元件(启动子、增强子、沉默子等);
存大量DNA多态性(SNP、串联重复序列多态性等);
具端粒结构。
端粒为真核生物线性基因组DNA末端特殊结构,DNA序列段与蛋白质形成的复合体,序列保守
保护线性DNA完整复制、保护染色体末端、决定细胞寿命等
3.1.1.2. 原核基因组¶
基因组小、常仅一条染色体,DNA量少。细菌质粒、真核生物线粒体、叶绿体等含DNA及功能基因,称染色体外遗传因子。
基因组特点:
结构简练(绝大部分用于编码蛋白质,仅少部分不转录);
存在转录单元(功能相关RNA、蛋白质基因结合于基因组某些特定部位形成功能单位/转录单元;可转录为含多mRNA分子,即多顺反子);
具重叠基因(同段DNA可携带不同蛋白质信息)。
3.1.2. DNA结构¶
3.1.2.1. 一级、二级结构¶
一级结构:
4种核苷酸连接、排列顺序(DNA分子的化学构成);
常为线性、环状,绝多数为两互补双链,少数如某些噬菌体、病毒为单链;
决定高级结构,高级结构影响、决定一级结构功能。
二级结构:
两条多核苷酸链反向平行盘绕成双螺旋结构(特点:由两互相平行的脱氧核苷酸链盘绕成;脱氧核糖、磷酸交替连接于外侧成骨架,碱基于内侧);
两链上碱基经氢键结合成碱基对,嘌呤与嘧啶配对(A-T、C-G,碱基互补配对原则)。
双螺旋 |
A-DNA |
B-DNA |
Z-DNA |
|---|---|---|---|
碱基倾角/° |
20 |
6 |
7 |
碱基间距/nm |
0.26 |
0.34 |
0.37 |
螺径/nm |
2.55 |
2 |
1.84 |
每圈碱基对 |
11 |
10 |
12 |
大沟 |
狭、深 |
宽、较深 |
平坦 |
小沟 |
宽、浅 |
狭、较深 |
狭、深 |
糖苷键构象 |
反式 |
反式 |
C反、G顺 |
螺旋反向 |
右 |
右 |
左 |
A-DNA:较B-DNA,碱基倾斜大,偏向双螺旋边缘,具深窄大沟、宽浅小沟;DNA双链种任一链被相应RNA替换则变为A-DNA(转录时等)。
Z-DNA:邻近调控模式 图 3.1.2 Ⅰ,与调节区相邻的转录区被Z-DNA抑制,转为B-DNA后活化;远距离调控模式 图 3.1.2 Ⅱ,Z-DNA经增加负超螺旋,调节聚合酶与模板链结合而调节转录起始活性(B-DNA时,远距转录区负超螺旋水平低,无扭转张力)。
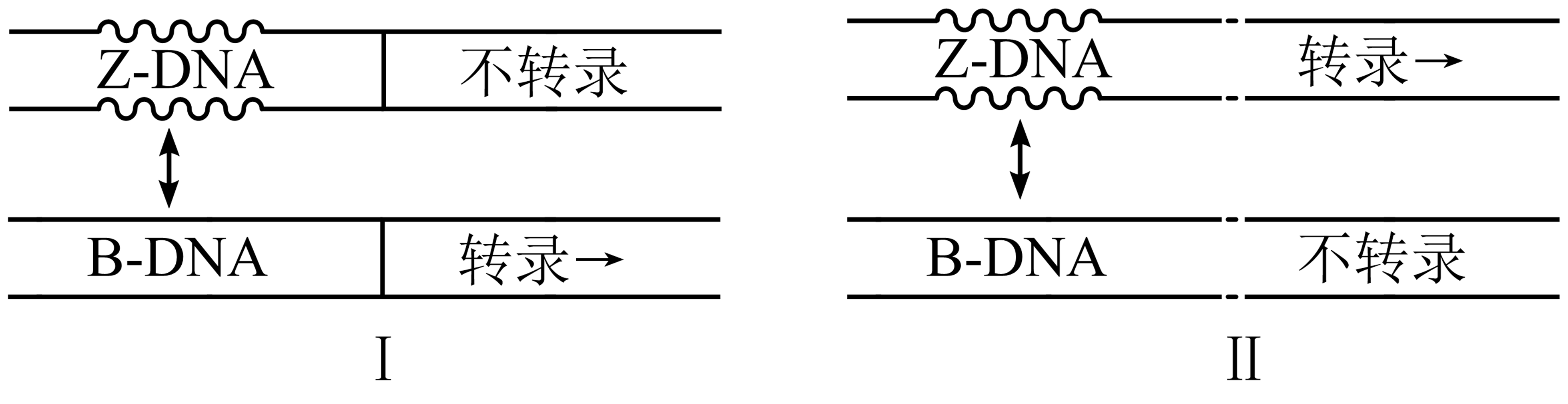
图 3.1.2 Z-DNA调节模式¶
变性与复性:
双螺旋链间经非共价键结合易分开;
当DNA溶液温度接近沸点、pH较高时,两互补链可分开,称DNA变性;
变性过程可逆,当DNA溶液缓慢降温,互补链可重新聚合形成规则双螺旋(复性)。
增色效应:DNA溶液升温近沸点时,260nm吸光度明显增加;减色效应:双螺旋DNA碱基堆积降低光吸收能力。
DNA接连温度/熔点:Tm,吸光度增加至最大值一半时候的温度;因素:G+C量高则Tm高,溶液离子强度,DNA均一性。
3.1.2.2. 高级结构¶
高级结构含:
超螺旋(主要形式;正超螺旋:右手超螺旋,过度缠绕双螺旋;负超螺旋:左手超螺旋,胞内常见形式)、
线性双链纽结、
多重螺旋等。
在电场作用下,同分子量时,分子迁移率:超螺旋DNA链>线性DNA>开环DNA。
超螺旋变化:L=T+W;连环数(L):环形DNA两链交叉次数,不发生链断裂时为常量;扭转数(T):双螺旋盘绕数;超螺旋数(缠绕数,W)为变量。
3.1.3. DNA复制¶
遗传实质为染色体DNA复制的结果;通过自我复制,主要为半保留复制;双链DNA复制阶段:起始、延伸、终止,需多种酶、蛋白质协同(拓扑异构酶、解旋酶、单链结合蛋白、引物合成酶、DNA聚合酶、连接酶等)。
半保留复制:复制时,氢键断裂、双链解旋,分别作为模板合成新链,使得子代DNA中一条链源自亲代,另一条为新合成。
复制子:
体内可独立进行复制的单位;
从复制起始点至终止点的区域;
一个复制子仅含一个复制起始点。
复制叉:
复制时双链DNA解旋,复制起点呈叉子形式;
从复制起始点处沿DNA链移动,单向复制时产生单个复制叉,双向复制时产生两个复制叉从起始点沿相反方向等速前进。
复制起始点:
细菌、酵母、线粒体、叶绿体的起始点含丰富AT序列利于解链,常为单复制子;
真核生物中具多复制子,但非同时作用。
复制终止点:复制子中控制复制终止的位点。
复制方向:
单向复制(从一个复制起始点始,仅一个复制叉移动);
双向复制(复制起始点两侧形成复制叉,相反方向移动);
相向复制(特殊复制模式,两个复制起始点分别起始两条链复制,两个复制叉中仅分别合成一条链,相向移动)。
复制速率:真核生物因具复杂高级结构(复制时需解开核小体,复制后需形成核小体)速率较原核生物慢,但具多个复制起始点可进行多复制子同步复制。
半不连续复制:
DNA双螺旋链反向平行(一条5’→3’、另一条3’→5’),但DNA聚合酶合成方向均为5’→3’;
合成时双链分前导链(合成方向5’→3’,连续复制)、后随链(模板DNA链暴露后,以与复制叉移动相反方向按5’→3’合成冈崎片段后再连接而成)。
3.1.3.1. 主要复制形式¶
线性DNA双链复制:单起点单向/双向、多起点双向。
因线性DNA复制时,RNA引物切除后的缺失可经以下途径复制:
线性复制子转为环状、多聚分子;
DNA末端成发夹结构;末端蛋白介入。
环状DNA双链复制:θ型、滚环型、D环型。
3.1.3.2. 原核复制特点¶
解旋:先拓扑异构酶Ⅰ解开负超螺旋,与解链酶(经水解ATP供能,大部分沿后随链模板5’→3’方向移动,仅Rep蛋白沿前导链模板3’→5’方向移动)共同作用解开双链;解链后由SSB蛋白(单链结合蛋白,保持单链结构)结合稳定单链;引发体结合于链上。
引发:引发酶于DNA模板合成小段RNA链;后随链的引发由引发体完成。
延伸:前导链:持续合成;后随链:引物合成、延伸、去除引物、连接。
终止:复制叉移至终止子时,Ter-Tus复合物使DnaB脱离抑制解链,阻挡复制叉移动;终止后未复制的序列经修复机制填补。
DNA聚合酶表 8 4:DNA聚合酶Ⅰ非主要聚合酶,C端区域具聚合酶活性、3’→5’外切酶活性;N端区域具5’→3’ 外切酶活性(切除嘧啶二聚体);可去除冈崎片段5’RNA引物。DNA聚合酶Ⅱ具5’→3’聚合酶活性,但活性低,仅Ⅰ的5%;其3’→5’外切酶活性可起校正作用;主要起修复DNA作用。DNA聚合酶Ⅲ具5’→3’聚合酶活性、3’→5’外切酶活性;活性较强,延长反应的主导酶。DNA聚合酶Ⅳ、Ⅴ主要在SOS修复过程中发挥作用。
性质 |
DNA polⅠ |
DNA polⅡ |
DNA polⅢ |
|---|---|---|---|
3’→5’ |
+ |
+ |
+ |
5’→3’ |
+ |
- |
- |
新链合成 |
- |
- |
+ |
滑动DNA夹结合使得DNA聚合酶于复制叉上具高延伸性,保持酶与DNA的接触,增加持续合成能力。
3.1.3.3. 真核复制特点¶
真核生物染色体具多复制起始点,复制完成前各起始点DNA复制不能开始,复制为细胞周期的一部分(S期)。
自主复制序列:ARS,复制起始点。
复制起始需起始点识别物(ORC)参与。
复制叉移动速度慢,每30k~300kbp分布一个复制起始点。
性质 |
α |
β |
γ |
δ |
ε |
|---|---|---|---|---|---|
亚基数 |
4 |
1 |
2 |
2/3 |
≥1 |
分布 |
核 |
核 |
线粒体 |
核 |
核 |
功能 |
DNA引物合成 |
损伤修复 |
MitoDNA复制 |
主要DNA复制酶 |
复制修复 |
3’→5’外切 |
- |
- |
+ |
+ |
+ |
5’→3’ 外切 |
- |
- |
- |
- |
- |
真核DNA聚合酶性质与细菌DNA聚合酶相似,均以dNTP为底物,需Mg2+激活。
复制叉上具聚合酶α(或引发酶复合体)及两聚合酶(δ+δ/ε;前者延伸前导链,后者合成后随链冈崎片段)。
冈崎片段切除:RNA酶H1切除后由DNA连接酶Ⅰ连接相邻冈崎片段。后随链末端的序列缺失,通过端粒结构及具反转录活性端粒酶恢复。
3.1.3.4. 调控¶
E.coli:主要发生于起始阶段;调控模式与操纵子类似;起始物位点突变使得复制停止、细胞死亡。复制的起始不依赖细胞分裂,复制终止则引发细胞分裂。
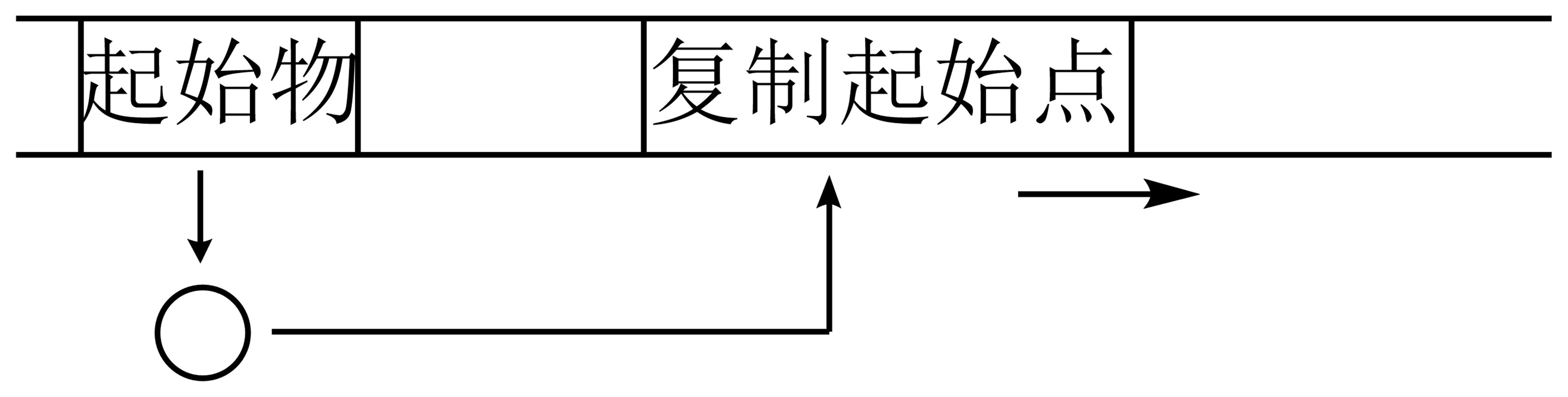
图 3.1.3 E.coli复制调控模式¶
真核细胞:细胞周期水平(限制点调控,决定细胞是否进入S期);染色体水平(决定复制子起始顺序);复制子水平(决定复制起始)。
3.1.4. DNA修复¶
染色体DNA具重要作用,复制准确性、损伤修复具重要意义。
DNA修复系统 |
功能 |
|---|---|
错配修复 |
修复错配碱基 |
切除修复 |
切除突变碱基、片段 |
重组修复 |
复制后修复,重启停滞复制叉 |
DNA直接修复 |
修复嘧啶二聚体、甲基化DNA |
SOS系统 |
应急修复,导致变异 |
错配修复:
复制过程中发生错配,修复系统识别新链中的错配并校正;
模板链甲基化;
新链错配处由DNA外切酶Ⅶ(上游母链甲基化位点至错配点)或外切酶Ⅰ/Ⅹ(错配点至下游母链甲基化位点)切除后经DNA聚合酶Ⅲ修复。
切除修复:
碱基切除修复(受损核苷酸可被特异性糖苷水解酶切除核苷酸N-β糖苷键形成去嘌呤/去嘧啶位点,即AP位点;
AP核酸内切酶切除含AP位点的小段DNA;DNA polⅠ合成新片段);
核苷酸切除修复(核苷酸损伤使得双链间无法形成氢键,切除含损伤位点片段后修复)。
重组修复:
复制后修复,对损伤部位先复制后修复;
修复时将同源DNA母链相应序列移至损伤处,后补母链空缺。
直接修复:
将损伤碱基修复为原状态;
DNA光解酶作用于嘧啶二聚体(光/紫外照射形成)。
SOS反应:
细胞DNA受损、复制系统受抑等紧急情况下的应急措施;
反应含DNA损伤修复、诱导效应、分裂抑制、溶源性细菌释放噬菌体等;
与细胞癌变相关;
广泛存在于真核、原核细胞:DNA修复、产生变异。
3.1.5. DNA转座¶
DNA转座:
移位,由可移位因子介导的遗传物质重排现象;
依赖DNA复制,新位点的序列可移位因子拷贝。
3.1.5.1. 分类及结构特征¶
转座子(Tn):存于染色体DNA上可自主复制、位移的基本单位;分两类:插入序列(IS)、复合型转座子。
插入序列:最简单转座子,无宿主基因;为细菌染色体、质粒DNA正常组成部分;末端具反向重复序列。
复合型转座子:一类带抗性基因转座子,两翼具相同/同源IS;IS序列移至功能基因两侧时形成复合体。
3.1.5.2. 真核转座子¶
真核细胞内转座子流动性可能高于原核生物。
在玉米细胞内,转座子具两大类:
自主性转座子(具自主剪接、转座功能;Ac-Ds系统)、
非自主性转座子(单独存在时稳定不转座,基因组中具同家族自主性转座子时才可转座;Ds元件)。
3.1.5.3. 机制及效应¶
转座可分复制型(转座酶:原始转座子;解离酶:复制转座子)、非复制型(原始转座子以移动实体直接移位)。
转座插入时,受体靶序列DNA被复制,分布于转座子两侧。
效应:
引起插入突变;
产生新基因;
产生染色体畸变(重组发生于正向重复转座间引起缺失、重组发生于反向重复转座间引起倒位);
引起进化。
3.1.6. SNP¶
单核苷酸多态性(SNP):基因组DNA序列由于单个核苷酸突变引起的多态性;可能为转换、颠换。
检测:基因芯片、Taqman技术、分子导标技术、焦磷酸测序法等。
应用:人单倍体型图绘制、疾病易感基因相关性分析、用药及药物设计。